Vsebina
- Glavna razlika
- Primerjalna tabela
- Kaj so jonske spojine?
- Kaj so molekularne spojine?
- Ionske spojine v primerjavi z molekularnimi spojinami
Glavna razlika
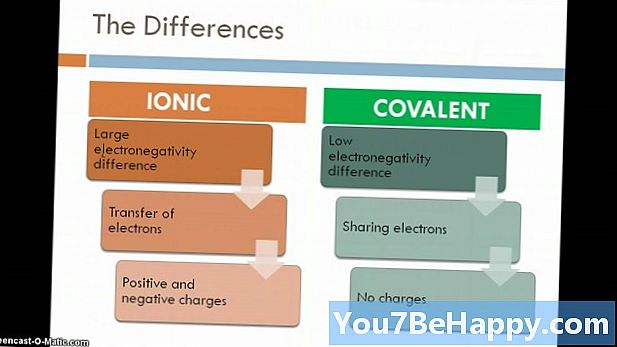
Spojina je prepoznana kot snov, ki nastane, kadar se dva ali več elementov združujejo v določenih razmerjih s pomočjo kemične vezi. Ionska spojina je spojina, ki nastane zaradi elektrostatične privlačne sile med kovinami in nekovinami. Običajno se ionske spojine pojavijo v prodanem kristalnem stanju. Ionske spojine so tudi dobri vodniki električne energije in imajo visoke tališča in vrelišča. Po drugi strani pa se molekularne spojine tvorijo zaradi delitve elektronov med dvema nekovinama. Glede na ionske spojine so slab prevodnik električne energije in imajo nizko tališče in vrelišče.
Primerjalna tabela
| Ionske spojine | Molekularne spojine | |
| Tvorba | Ionske spojine nastanejo zaradi elektrostatične privlačne sile med kovinami in nekovinami. | Molekularne spojine nastanejo zaradi delitve elektronov med dvema nekovinama. |
| Skupina | Ionske spojine nastajajo med kovinskimi in ne mentalnimi. | Molekularne spojine nastanejo, kadar se dve nekovini kemično združita |
| Bond | Ionska spojina nastane zaradi elektrostatične privlačne sile, znane kot jonska vez. | Molekularne spojine nastanejo zaradi kovalentne vezi med elementi. |
| Tališče in vrelišče | Visoka | Nizka |
| Država | Ionske spojine so vedno v trdnem stanju z oblikovanjem kristalnega videza. | Molekularne spojine so lahko v katerem koli stanju, trdne, tekoče ali plinske pri sobni temperaturi. |
| Dirigent električne energije | Dobro | Slab |
Kaj so jonske spojine?
Te spojine nastanejo zaradi elektrostatične sile privlačnosti med kovinami in nekovinami. Z enostavnejšimi besedami sila (ionska vez) pri tem pozitivno in negativno nabito reagira skupaj, da tvori spojino. Običajno se ionske spojine pojavljajo v prodanem kristalnem stanju in so dobri prevodniki električne energije, ki imajo visoke tališča in vrelišča. Ionske spojine nastajajo med kovinami in nekovinami ter imajo nekakšen sijoč videz.
Primer: Namizna sol (NaCl) je najpogostejši primer jonske spojine. Natrij (NA) je v tej tvorbi kovina, medtem ko je klor (Cl) nekovina, oba pa sta zaradi elektrostatične sile privlačenja med seboj skupaj.
Kaj so molekularne spojine?
Spojine, ki nastanejo zaradi delitve elektronov med nekovinami, so znane kot Molekularna spojina. Elementi, ki tukaj reagirajo, so združeni zaradi kovalentne vezi, zato se te spojine pogosto imenujejo kovalentne spojine.Glede na ionske spojine so slab prevodnik električne energije in imajo nizko tališče in vrelišče.
Primer: V ozonu (O3) se kisik kombinira z deljenjem elektronov in tvori ozon.
Ionske spojine v primerjavi z molekularnimi spojinami
- Ionske spojine nastanejo zaradi elektrostatične privlačne sile med kovinami in nekovinami, medtem ko se molekularne spojine tvorijo zaradi delitve elektronov med dvema nekovinama.
- Molekularne spojine nastanejo, kadar se dve nekovinski kemično združita, po drugi strani pa se ionske spojine tvorijo med kovino in nemetalno.
- Molekularne spojine nastanejo zaradi kovalentne vezi med elementi, medtem ko se ionska spojina tvori zaradi elektrostatične privlačne sile, znane kot jonska vez.
- Molekularne spojine imajo v primerjavi z jonskimi spojinami nizko tališče in vrelišče.
- Molekularne spojine so lahko v kateri koli stanju, trdne, tekoče ali plinske pri sobni temperaturi, medtem ko so ionske spojine vedno v trdnem stanju in tvorijo kristalni videz.
- Molekularne spojine so slab prevodnik električne energije, medtem ko so jonske spojine dober prevodnik električne energije.